- Haben Sie noch Fragen? Kontaktieren Sie uns
- info@dr-rath-foundation.org

Jean-Claude Junckers Rede zur ‚Lage der Union’ – „Musizieren während Rom brennt“
September 19, 2016
Microsoft schreibt sich die „Lösung“ des Krebsproblems binnen 10 Jahren auf die Fahne, lässt aber die Hauptursache der Krankheit unerwähnt
September 26, 2016Eine spezifische Kombination aus Ascorbinsäure, Lysin, Prolin und Epigallocatechin-Gallat hemmt die Ausbreitung und die Invasion der extrazellulären Matrix verschiedener Krebszelllinien beim Menschen
Shrirang P Netke, M Waheed Roomi, Vadim Ivanov, Aleksandra Niedzwiecki* und Matthias Rath
Emerging Drugs, Vol. II. 2003, 37-50
Matthias Rath, Inc., Research and Development, Santa Clara, CA 95054
* Autor für Korrespondenz und Nachdrucke. Telefon: (408) 807-5564, Fax: (408) 986-9403
Schlüsselwörter: antiproliferative und antimetastatische Wirkung, Brustkrebs (MDA-MB-231), Dickdarmkrebs (HCT116), Epigallocatechin-Gallat, Gelatinase-Zymographie, Matrix-Metalloproteinasen (MMP)-2 und -9, Ausbreitung von Krebs, Hautmelanom (A2058), spezifische Kombination aus Ascorbinsäure, Prolin und Lysin.
Zusammenfassung
Wir haben festgestellt, dass eine bestimmte Kombination aus Ascorbinsäure (AA, 100 µM), Prolin (P, 140 µM) und Lysin (L, 400 µM) eine signifikante antiproliferative und antimetastatische Wirkung auf einige menschliche Krebszelllinien, Brustkrebs (MDA-MB-231), Dickdarmkrebs (HCT116) und Hautkrebs (Melanom, A2058) hatte. In Gegenwart dieser Nährstoffkombination wurde die Invasion der extrazellulären Matrix durch menschliche Brustkrebszellen, Melanomzellen und Dickdarmkrebszellen um 50 %, 10 % bzw. 30 % gehemmt. Die Zugabe von Epigallocatechin-Gallat (EGCG) verbesserte diese Ernährungssynergie weiter und führte zu einer noch deutlicheren hemmenden Wirkung sowohl bezüglich der Zellausbreitung als auch bezüglich der Matrixinvasion. Im Vergleich zum Medium ohne zugegebene Nährstoffe wurde die Ausbreitung von Brustkrebszellen MDA-MB-231 in Gegenwart von A, P, L und 20 µg/ml EGCG auf 74 % und von Dickdarmkrebszellen HCT116 auf 69 % verringert. Die Erhöhung der EGCG-Konzentration auf 50 µg/ml brachte keine weitere Verringerung der Zahl der Brustkrebszellen. Jedoch wurde dadurch bei der Kontrollgruppe die Ausbreitung von Dickdarmkrebszellen auf 4,6 % und von Melanomzellen auf 30 % gesenkt. Die Matrigel-Invasion durch Brustkrebszellen und menschliche Melanomzellen in Gegenwart von AA, P, L und 20 µg/ml EGCG wurde vollständig gestoppt. Bei gleicher Konzentration wurde die Invasion durch Dickdarmkrebszellen auf 24,9 % reduziert. Wie die Gelatinase-Zymographie zeigt, wurde die Expression von Matrix-Metalloproteinasen (MMP)-2 und -9 durch diese Nährstoffkombination in Melanomzellen allerdings nicht verändert. MMP-2 und MMP-9 wurden durch EGCG dosisabhängig gehemmt; L, P und AA zeigten keine zusätzliche Wirkung. Somit bietet die Kombination aus AA, P, L und EGCG ein großes Potenzial für die Kontrolle von Krebs durch ein sicheres und vielseitig wirksames Verfahren.
Einleitung
Einer der Hauptmechanismen, den Krebszellen verwenden, um sich im Körper auszubreiten und Metastasen zu bilden, ist die enzymatische Zerstörung des umliegenden Bindegewebes. Therapeutische Maßnahmen zur Kontrolle dieses Prozesses durch spezielle Medikamente haben nicht zum Erfolg geführt und zurzeit gibt es kein Mittel, um die Metastasenbildung von Krebs zu kontrollieren. Aktuelle Behandlungsmethoden konzentrieren sich mit Chemotherapie und Strahlentherapie auf die Zerstörung der Krebszellen im Körper; sie richten sich nicht gegen die Metastasenbildung. Darüber hinaus sind diese Behandlungen toxisch, nicht spezifisch und mit schweren Nebenwirkungen verbunden. Chemotherapie und Strahlentherapie bergen das Risiko der Entwicklung neuer Krebsarten und können durch die Zerstörung des Bindegewebes im Körper die Invasion von Krebs erleichtern. Aus diesem Grund werden sichere und wirksame Naturheilverfahren benötigt, die zur Kontrolle der Krebsausbreitung im Körper eingesetzt werden können.
Um zu wachsen und sich in andere Bereiche des Körpers auszubreiten, bauen die Krebszellen die extrazelluläre Matrix (ECM) durch verschiedene Matrix-Metalloproteinasen (MMP) und Plasmin ab, deren Aktivitäten mit einem aggressiven Tumorwachstum einhergehen. Rath und Pauling (1992) postulierten, dass Nährstoffe wie eine Aminosäure, Lysin und Ascorbinsäure als natürliche Inhibitoren für die Proteolyse der extrazellulären Matrix fungieren können und das Potenzial besitzen, das Tumorwachstum und die Tumorausbreitung zu steuern. Diese Nährstoffe können ihr Anti-Tumor-Potenzial durch verschiedene Mechanismen umsetzen, z. B. durch die Hemmung von MMP und durch die Stärkung des Bindegewebes, das die Krebszellen umgibt (Einkapselung des Tumors).
Im Rahmen der vorliegenden Studie haben wir die Wirkung von Lysin, Ascorbinsäure und Prolin hinsichtlich ihres antiproliferativen und anti-invasiven Potenzials in verschiedenen menschlichen Krebszelllinien untersucht. Darüber hinaus haben wir auch die Wirkung von Epigallocatechin-Gallat (EGCG) mit der vorstehend beschriebenen Kombination erforscht. EGCG ist für seine Antikrebswirkung in verschiedenen Human- und experimentellen Studien bekannt (Mukhtar und Ahmed, 2000, Valcic, Timmerman et al., 1996). Es wurde auch postuliert, dass eine solche Kombination aus Nährstoffen eine äußerst starke synergistische Wirkung ausüben würde.
Materialien und Methoden
Menschliche Brustkrebszellen MDA-MB-231, menschliche Dickdarmkrebszellen HCT116 und die menschliche Melanomzelllinie A2058 wurden von ATCC und normale menschliche Hautfibroblasten von Gibco bezogen. Wo keine speziellen Angaben gemacht werden, wurde das Kulturmedium von ATCC verwendet.
In den Untersuchungen zur Krebszellenausbreitung wurde jede Behandlung acht Mal wiederholt. Bei den Invasionsversuchen wurde jede Behandlung drei oder vier Mal wiederholt.
Untersuchung der Zellausbreitung
Bei diesen Untersuchungen wurden 5X 104-Brustkrebszellen in einem Liebovitz-Medium mit 10 % fötalem Rinderserum (FBS) in 24-Well-Platten gezüchtet. Das Medium wurde als solches (basal) oder mit bestimmten Zusätzen verwendet. Die Platten wurden vier Tage in einem Umluftinkubator (ohne zusätzliches CO2) inkubiert. Die Dickdarmkrebszellen HCT116 wurden in McCoy 5A-Medien gezüchtet und in einem Umluftinkubator mit 5% CO2 erhalten. Am Ende der Inkubationszeit wurden die Medien entnommen und die Zellen in den Wells mit PBS gewaschen. Anschließend folgte eine dreistündige Inkubation mit MTT-Färbung. Jedem Well wurde Dimethylsulfoxid (DMSO, 1 ml) zugegeben. Die Platten mit DMSO wurden unter vorsichtigem Rühren 15 Minuten lang Zimmertemperatur ausgesetzt. Danach wurde die OD der Lösung in jedem Well bei 550 nm gemessen. Die OD550 der DMSO-Lösung im Well wurde als direkt proportional zur Zahl der Zellen betrachtet. Die OD550 der Behandlung, die keine Zusätze enthielt (basal), wurde mit 100 angesetzt.
Untersuchung der Matrigel-Invasion
Die Untersuchungen wurden unter Verwendung von Matrigel-Einsätzen (Becton Dickinson) in kompatiblen 24-Well-Platten durchgeführt. Fibroblasten wurden in den Wells der Platte mit DMEM gesät und gezüchtet. Als die Fibroblasten Konfluenz erreicht hatten, wurde das Medium entnommen und durch 750 µl der für die Behandlung bestimmten Medien ersetzt. Die Krebszellen (5X 104), die in 250 µl des Mediums, das mit Nährstoffen entsprechend dem Aufbau des Experiments angereichert war, suspendiert worden waren, wurden auf den Einsatz im Well gesät. Somit enthielt das Medium sowohl auf dem Einsatz als auch im Well die gleichen Zusätze. Die Platten mit den Einsätzen wurden anschließend 18-20 Stunden inkubiert (die MDA-MB-231-Zellen in einem Umluftinkubator und die Dickdarmkrebszellen und Melanomzellen in einem 5 % CO2-Inkubator). Nach der Inkubation wurden die Medien aus den Wells genommen. Die Zellen auf dem oberen Bereich der Einsätze wurden vorsichtig mit einem Baumwolltupfer abgewischt. Die Zellen, die in die Matrigel-Membran eingedrungen und in den unteren Matrigel-Bereich gewandert waren, wurden mit Hemacolor (EM Sciences) gefärbt und visuell unter dem Mikroskop gezählt. Die Ergebnisse wurden einer ANOVA unterzogen und alle möglichen Paare wurde hinsichtlich ihrer Signifikanz bei p<0,05 getestet.
Die Medien in den verschiedenen Untersuchungen wurden mit Ascorbinsäure, Prolin, Lysin und EGCG in den Konzentrationen, die unter „Ergebnisse und Diskussion“ angegeben sind, angereichert.
Gelatinase Zymographie
Die Gelatinase-Zymographie erfolgte in 10 % vorgefertigtem Novex-Polyacrylamidgel (Invitrogen) in Gegenwart von 0,1 % Gelatine. Das Kulturmedium (20 µl) wurde eingebracht und es wurde eine SDS-PAGE mit Tris-Glysin-SDS-Puffer durchgeführt. Nach der Elektrophorese wurde das Gel 30 Minuten lang mit 5 % Triton X-100 gewaschen und gefärbt. Gleichzeitig wurde anhand von Proteinstandards die ungefähre Molekülmasse ermittelt.
Ergebnisse und Diskussion
(A) Untersuchung der Krebszellenausbreitung
Melanomzellen A2058
In Abbildung 1 ist die Wirkung von 10, 20 und 50 µg/ml EGCG ohne sowie mit der Zugabe von L, P und AA auf die Ausbreitung von Melanomzellen dargestellt. Weder L, P und AA noch EGCG hatten bei 10 und 20 µg/ml eine signifikante Wirkung auf die Zellausbreitung. EGCG verringerte jedoch bei 50 µg/ml die Zellzahl signifikant auf 30 %. Eine ähnliche Wirkung wurde bei der Zugabe von L, P und AA beobachtet.
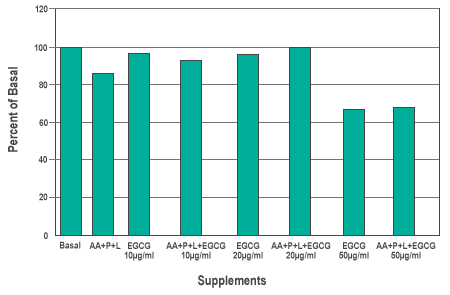
Abbildung 1: Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf die Zellausbreitung von Melanomzellen A2058.
Brustkrebszellen MDA-MB-231
Bei diesen Experimenten wurden dem basalen Medium 0, 10, 20, 50, 100 oder 200 µg/ml EGCG (Abb. 2) zugegeben. Die Ergebnisse zeigen, dass die Anreicherung des basalen Mediums mit 50, 100 und 200 µg/ml EGCG zu einer signifikanten Verringerung der Zellzahl auf 66,1 ± 5,3, 33,6 ± 2 bzw. 29,6 ± 0,8 % im Vergleich zu den Kontrollobjekten ohne Zusätze führte. Die EGCG-Konzentrationen im Zellmedium von bis zu 20 µg/ml hatten keine signifikante hemmende Wirkung auf die Zellausbreitung.
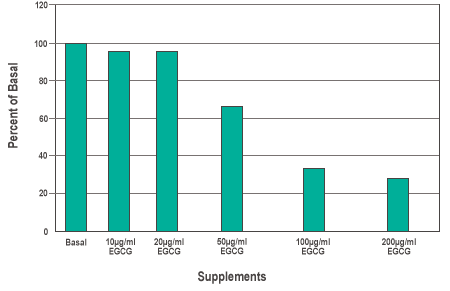
Abbildung 2: Die Wirkung von Epigallocatechin-Gallat (EGCG) auf die Zellausbreitung* von Brustkrebszellen MDA-MB-231.
Wir haben auch die Wirkung von AA, L und P sowie verschiedenen EGCG-Konzentrationen auf die Ausbreitung von Krebszellen untersucht. Abbildung 3 zeigt die nicht signifikante Verringerung der Zellzahl auf 86,1 + 1,93 % mit AA, L und P. Die Zugabe von 20, 50 und 100 µg EGCG zu dieser Kombination reduzierte die Zellzahl signifikant auf 74 ± 5,8, 64,8 ± 1,6 bzw. 22 ± 5 % im Vergleich zur Kontrollgruppe.
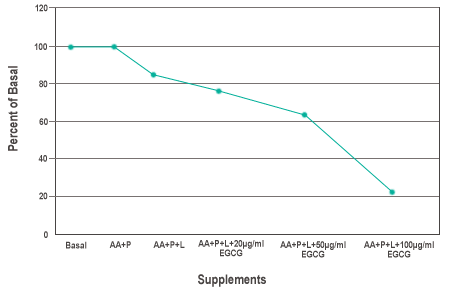
Abbildung 3 : Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf die Zellausbreitung von Brustkrebszellen MDA-MB-231.
Dickdarmkrebszellen HCT116
Während die hemmende Wirkung von AA, P und L auf die Zellausbreitung von Dickdarmkrebszellen nicht ausgeprägt war, verringerte die Kombination aus AA, P und L mit 20 µg/ml EGCG die Zellzahl signifikant auf 69 ± 0,5 % (Abb. 4). Eine höhere EGCG-Konzentration in dieser Kombination (50 µg/ml) reduzierte die Zellzahl drastisch auf 4,6 ± 0,3 %.
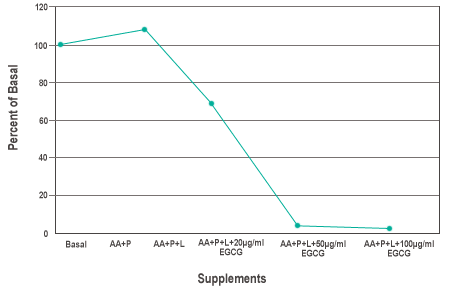
Abbildung 4: Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf die Zellausbreitung von Dickdarmkrebszellen HCT116.
Die antiproliferative Aktivität der Nährstoffkombinationen, die in diesen Untersuchungen verwendet wurden, variierte mit dem Typ der Krebszellen. Bei Brustkrebszellen hatte die Kombination aus AA, P und L mit EGCG eine größere antiproliferative Wirkung als bei der Einzelanwendung dieser Nährstoffe. Bei Melanom- und Dickdarmkrebszellen, die der Kombination aus AA, P und L ausgesetzt wurden, konnte keine Beeinflussung ihrer Ausbreitung beobachtet werden. Jedoch resultierte die Kombination dieser Nährstoffe mit 20 µg/ml EGCG in einer signifikanten Verringerung der Zahl der Dickdarmkrebszellen, allerdings nicht der Melanomzellen. Die Dickdarmkrebszellen reagierten empfindlicher als die Brustkrebs- und die Melanomkrebszellen auf die geringste Konzentration der Kombination aus AA, P, L und EGCG. Die Ausbreitung der Dickdarmkrebszellen wurde fast vollständig reduziert (4,6 %), als AA, P und L mit 50 µg/ml kombiniert wurden.
(B) Gelatinase-Zymographie
Die Wirkung von EGCG auf Melanomzellen mit Basal und mit den Zusätzen AA, P und L auf die Expression von MMP ist in Abbildung 5 anhand der Gelatinase-Zymographie dargestellt. Die Melanomzellen zeigten zwei Bänder, die MMP-2 und MMP-9 entsprachen. Die Kombination aus AA, L und P hatte, verglichen mit dem Basal, keine Wirkung auf die Expression der MMP-Bänder. EGCG hemmte jedoch dosisabhängig die Expression sowohl von MMP-2 als auch von MMP-9. Die Intensität der Bänder für Basal und die Kombination aus AA, L und P war identisch.
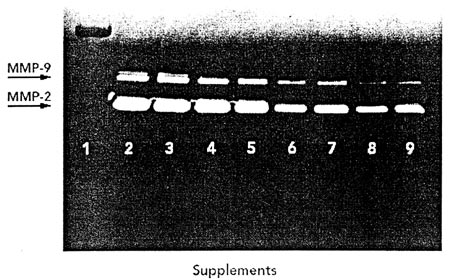
Abbildung 5: Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf die Expression von Matrix-Metalloproteinasen (MMP) durch Melanomzellen. 1. Marker, 2. Basal, 3. AA+P+L, 4. EGCG 10 µg/ml, 5. AA+P+L+10 µg/ml EGCG, 6. EGCG 20 µg/ml, 7. AA+P+L+EGCG 20 µg/ml, 8. EGCG 50 µg/ml, 9. AA+P+L+EGCG 50 µg/ml
(C ) Untersuchung der Invasion der extrazellulären Matrix und der Migration
Wir haben die hemmende Wirkung einer Kombination aus AA, P und L separat und zusammen mit EGCG-Konzentrationen auf die extrazelluläre Matrix unter Verwendung vorgeformter Matrigel-Matrizen, die routinemäßig zur Bestimmung des invasiven Potenzials verschiedener Krebszelllinien eingesetzt werden, untersucht.
Brustkrebszellen MDA-MB-231
In Abbildung 6 sind die Ergebnisse der Matrigel-Invasion von Brustkrebszellen, die in Gegenwart von AA, P und L inkubiert wurden, dargestellt. Die Invasion von Krebszellen, die in einer Kombination aus AA, P und L inkubiert wurden, wurde im Vergleich zu den Zellen, die in einem Medium ohne Zusätze inkubiert wurden, um 48,1 ± 22,1 % verringert. In den Medien, die nur mit 20 µg/ml EGCG angereichert waren, sank die Zahl der eindringenden Zellen auf 69,5 ± 27,4 %. Die vollständige Hemmung der Matrixinvasion durch Brustkrebszellen wurde in Gegenwart höherer EGCG-Konzentrationen (50 µg/ml und 100 µg/ml) erreicht.
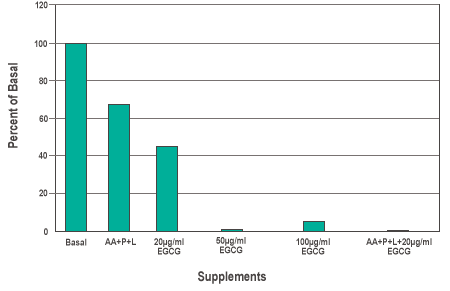
Abbildung 6: Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf die Matrigel-Invasion durch Brustkrebszellen MDA-MB-231.
Abbildung 6 zeigt darüber hinaus, dass die Kombination aus AA, P und L sowie 20 µg/ml EGCG die Invasion von Krebszellen durch die extrazelluläre Matrix vollständig gestoppt hat. Diese Kombination machte es möglich, die maximale hemmende Wirkung auf die Krebszelleninvasion zu erzielen, ohne dass dadurch einzelne Nährstoffe in hoher Konzentration benötigt wurden. Zusammen mit EGCG stoppten AA, P und L die Invasion von Brustkrebszellen vollständig bei einer geringeren EGCG-Konzentration (20 µg/ml).
Dickdarmkrebszellen HCT116
Abbildung 7 zeigt, dass die Kombination aus AA, P und L die Invasion von Dickdarmkrebszellen signifikant auf 67,2 ± 3,7 % reduzierte. Der alleinige Einsatz von EGCG in einer Konzentration von 20 µg/ml senkte die Invasion auf 44,9 ± 3,3 %, während die Kombination aus AA, P und L sowie 20 µg/ml EGCG einen synergistischen Effekt hatte und die Invasion der Dickdarmkrebszellen auf 24,9 ± 4,6% verringerte.
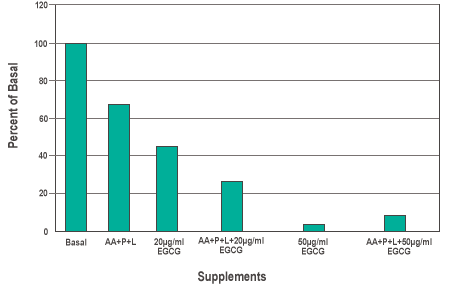
Abbildung 7: Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf die Matrigel-Invasion durch Dickdarmkrebszellen HCT116.
Melanomzellen A2085
Abbildung 8 zeigt, dass die Kombination aus AA, P und L die Zahl der eindringenden Zellen auf 88,2 ± 4% reduzierte. Diese Verringerung war jedoch nicht statistisch signifikant. Die Kombination dieser Nährstoffe mit nur 20 µg/ml EGCG führte zu einer wirksamen Senkung der Zahl der eindringenden Zellen auf Null.
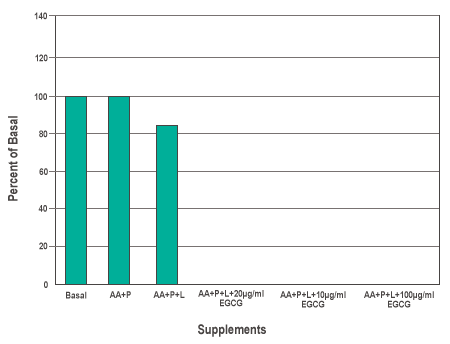
Abbildung 8: Die Wirkung der Anreicherung von Basal mit 100 µM Ascorbinsäure (AA), 140 µM Prolin (P) und 400 µM Lysin (L) sowie mit verschiedenen Konzentrationen von Epigallocatechin-Gallat (EGCG) auf Matrigel.
Diese Ergebnisse zeigen, dass wir durch die Verwendung von AA, P und L mit EGCG eine drastische Reduzierung der Zahl der Zellen erreichen konnten, die bei niedrigeren EGCG-Konzentrationen durch die Matrigel-Membran eindrangen und migrierten. Die Invasion wurde bei Brustkrebszellen und Melanomzellen mit einer geringen EGCG-Konzentration von 20 µg/ml und einer Kombination aus AA, P und L auf Null verringert. Die Vorteile der Kombinationsergebnisse waren bei Dickdarmkrebszellen nicht so spektakulär wie bei Brustkrebszellen. Die EGCG-Konzentration musste auf 50 µg/ml erhöht werden, um eine 90 %-ige Reduzierung der Invasion durch diese Zellen zu erzielen. Im Rahmen der vorliegenden Studie haben wir keine Veränderung der MMP-Expression bei Melamonzellen beobachtet, obwohl EGCG dosisabhängig eine hemmende Wirkung auf ihre Expression hat.
Ziel dieser Studie war es, die Nährstoffkombination mit der effektivsten antiproliferativen und anti-invasiven Wirkung auf Krebszellen zu ermitteln. Die Untersuchung der molekularen Mechanismen muss in einem zweiten Schritt erfolgen. Wir können hier mehrere Mechanismen postulieren, anhand derer die hemmende Wirkung der beteiligten Nährstoffe untersucht werden kann.
Die MMP-Aktivität lässt sich mit Lysin durch plasmininduzierte Mechanismen beeinflussen, obschon andere Mechanismen nicht ausgeschlossen werden. Die MMP werden als Proenzyme ausgeschieden. Ihre Aktivierung wird teilweise durch Plasmin bedingt und ihre Vollendung erfordert eine aktive Form von MMP-3. Der Aktivierungsmechanismus verschiedener MMP, der von Nagase beschrieben wird (1997), weist darauf hin, dass für MMP-3 ebenfalls die Umwandlung von Plasminogen in seine aktive Form Plasmin erforderlich ist. Das aktive Bindungszentrum von Plasminogen besitzt die Stellen, an denen sich Lysin vor allem anhängt. Aus diesem Grund kann Lysin die Aktivierung von Plasminogen in Plasmin durch den Plasminogenaktivator (Rath und Pauling, 1992) stören, indem es sich an plasminogenaktive Stellen heftet. Tranexamsäure, ein synthetischer Lysin-Analogstoff, wurde verwendet, um die plasmininduzierte Proteolyse durch diesen Mechanismus zu hemmen.
Da die Plasminaktivität von wesentlicher Bedeutung für die Induzierung verschiedener Gewebe-MMP ist, kann Lysin die Umwandlung von Plasminogen in Plasmin stören und dadurch die Aktivierung fast sämtlicher MMP verhindern. Darüber hinaus hat sich gezeigt, dass EGCG durch die Inhibition von MMP-2 eine hemmende Wirkung auf den Abbau der extrazellulären Matrix hat (Demeule et al., 2000).
Es ist auch möglich, die Invasion der Zellmatrix zu beeinflussen, indem man die Stabilität und die Stärke des Bindegewebes, das die Krebszellen umgibt, erhöht und die „Einkapselung“ des Tumors fördert. Dies erfordert die Optimierung der Synthese und der Struktur der Kollagenfibrillen, für die die Hydroxylierung von Hydroxyprolin- und Hydroxylysinresten in den Kollagenfibrillen von größter Wichtigkeit ist. Es ist bekannt, dass Ascorbinsäure unerlässlich für die Hydroxylierung dieser Aminosäuren ist. Ascorbinsäure und L-Lysin werden in der Regel nicht im menschlichen Körper produziert. Daher sind suboptimale Konzentrationen dieser Nährstoffe in verschiedenen pathologischen Stadien sowie durch eine unausgewogene Ernährung möglich. Obwohl Prolin aus Arginin synthetisiert werden kann, werden seine Synthese und/oder Hydroxylierung unter Umständen durch pathologische Zustände beeinflusst. Es hat sich gezeigt, dass der Hydroxyprolingehalt von metastatischem Tumorgewebe wesentlich geringer ist als in nicht metastatischem Tumorgewebe (Chubainskaia et al., 1989). Eine Vielzahl von Medikamenten, die die Metastasierung verringert haben, haben gleichzeitig den Hydroxyprolingehalt der Gewebe erhöht (Chubainskaia et al., 1989). Die Hydroxyprolinkonzentration im Urin von Krebspatienten war höher als bei gesunden Personen oder Patienten ohne Krebs (Okazaki et al., 1992). All diese Ergebnisse lassen eine nachteilige Wirkung von Krebszellen auf den Prolinmetabolismus sowie einen möglichen konditionierten Prolinmangel bei Krebspatienten vermuten.
Bei Krebspatienten wurden geringere Ascorbinsäurekonzentrationen festgestellt. (Anthony und Schorah, 1982, Nunez et al., 1995, Kurbacher et al., 1996). Ascorbinsäure ist äußerst zytotoxisch für bösartige Zelllinien (Koh et al., 1998, Roomi et al., 1998) und wirkt antimetastatisch (Liu et al., 2000). Unsere Untersuchungen anhand der Kombination aus Ascorbinsäure, Prolin und Lysin haben ergeben, dass diese Kombination eine starke antiproliferative und antimetastatische Wirkung auf verschiedene Krebszelllinien in Gewebekulturstudien hat. Die Wirkung konnte jedoch die Ausbreitung und Metastatisierung nicht völlig verhindern.
EGCG, eines der Catechine im Extrakt des grünes Tees, ist das stärkste Antikrebsmittel (Valcic et al., 1996, Mukhtar und Ahmed, 2000). Es wirkt auf bestimmte menschliche Krebszelllinien wachstumshemmend. (Ahmad et al., 1997, Liang et al., 1997, Yang et al., 1998). Es besteht also eine Synergie in den Antikrebsaktivitäten der Kombination aus AA, P und L einerseits und EGCG andererseits. Aus diesem Grund nahm man an, dass diese Kombination zusammen mit EGCG eine synergistische Antikrebsaktivität entwickeln würde.
Es steht fest, dass die Kombination aus AA, P und L mit EGCG das Potenzial besitzt, bei allen drei Krebsarten, die im Rahmen der vorliegenden Studie untersucht wurden, zu einer wesentlichen Verbesserung beizutragen. Bei Brustkrebs und Melanomen wird diese Verbesserung durch die drastische Verringerung der Zellmetastatisierung erreicht. Bei Dickdarmkrebs kann mit einer höheren EGCG-Konzentration eine erhebliche Reduzierung der Ausbreitung und der Metastatisierung erzielt werden.
Literaturverzeichnis
Ahmad, N., Feyes, D.K., Nieminen, A.L., Agarwal, R. and Mukhtar, H. (1997). Green tea constituent epigallocatechin-3-gallate and induction of apoptosis and cell cycle arrest in human carcinoma cells J.Natil. Cancer Inst. 89: 1991-1886.
Anthony, H.M. and Schorah, C.J. (1982) Severe hypovitaminosis C in lung-cancer patients: The utilization of vitamin C in surgical repair and lymphocyte related host resistance. Br. J.Cancer 46: 354-367.
Chubinskaia, S.G., Sevastìanova, N.A., Veksler, I.G. and Slutskii, L.I. (1989) Biochemical changes in the connective tissue components of malignant tumors and lungs in mice during metastatic spreading and chemotherapy. Vopr. Med. Kim. 35: 30-34.
Demeule, M., Brossard, M., Pahe, M., Gingras, D. and Beliveau, R. (2000) Matrix metalloproteinase inhibition by green tea catechin. Biochim. Biophys. Acta. 1478: 51-60.
Koh, W.S., Lee, S.J., Lee, H., Park, C., Park, M.H., Kim, W.S., Yoon, S.S., Park, K., Hong, S.S., Chung, M.H. and Park, C.H. (1998) Differntial effects and transport kinetics of ascorbate derivatives in leuckemic cell lines. Anticancer Re. 8: 2487-2493.
Kurbacher, C.M., Wagner, U., Kolster, B., Andreotti, P.E., Krebs, D. and Bruckner, H.W. (1996) Ascorbic acid (vitamin C) improves the antineoplastic activity of doxorubicin, cisplatin and paclitaxel in human breast carcinoma cells in vitro. Cancer. Lett. 103: 183-189
Liang, Y.C., Lin-shiau, S.Y., Chen. C.F. and Lin, K.J. (1997) Suppression of extracellular signals and cell proliferation through EGF receptor binding (-) epigallocatichin gallate in human A43 epidermal carcinoma cells. J. Cell. Bioechem 67: 55-65.
Liu, J.W., Nagao, N., Kageyama, K. and Miwa, N. (2000) Anti-metastatic effect of an antooxidation-resistant and lipophilic ascorbic acid derivative through inhibition of tumor invasion. Anticancer. Res. 20: 113-118.
Muktar, H. And Ahmed, N. (2000). Tea polyphenols: prevention of cancer and optimising health. Am. J. Clin. Nutr. 71: 1698S-1720S.
Nagase, H. (1997). Activation mechanisms of matrix metalloproteinases. Bio Chem. 378:51-160.
Nunez, M.C., Ortiz de Apodaca, Y. and Ruiz, A. (1995). Ascorbic acid in the plasma and blood cells of women with breast cancer. The effect of consumption of food with an elevated content of this vitamin. Nutr. Hosp. 10; 368-37
Okazaki, I., Matsuyama, S., Suzuki, F., Maruta, A., Kubochi, K., Yoshino, K., Kobayashi, Y., Abe, O. and Tsuchiya, M. (1992). Endogenous urinary 3-hydroxyproline has 96% specificity and 44% sensitivity for cancer screening. Lab. Clin. Med. 120: 828-830.
Roomi, M.W., House, D., Eckert-Macksic, M., Maksic, Z.B. and Tsao, S.C. (1998). Growth, suppression of malignant leukaemia cell line in vitro by ascorbic acid (vitamin C) and its derivatives. Cancer. Letters.122: 93-99.
Rath, M. and Pauling, L. (1992) Plamin induced proteolysis and role of apoprotein(a), lysine and synthetic lysine analogs. J. Orthomolecular. Medicine. 7:17-23.
Valcic, S., Timmermann, B.N., Alberts, D.S., Wachter, G.A., Krutzsch, M., Wymer, J. and Guillen, M. (1996), Inhibitory effects of six green tea-catechins and caffeine on the growth of four selected human tumor cell lines. Anticancer Drugs 7: 461-468.
Yang, G.Y., Liao, J., Kim, K., Yurkow, E.J. and Yang, C.S. (1998) Inhbition of growth and induction of apoptosis in human cancer cell lines by tea polyphenols. Carcinogenesis.19: 611-616


